Atomene som dannes i radioaktive prosesser er ofte selv radioaktive, og vil i så fall desintegrere videre under utsendelse av enten α- eller β-partikler. Dette fortsetter helt til det dannes et stabilt, ikke-radioaktivt atom. På denne måten kan man beskrive serier av radioaktive atomer som tilhører forskjellige grunnstoffer der de enkelte ledd er genetisk forbundet med hverandre.
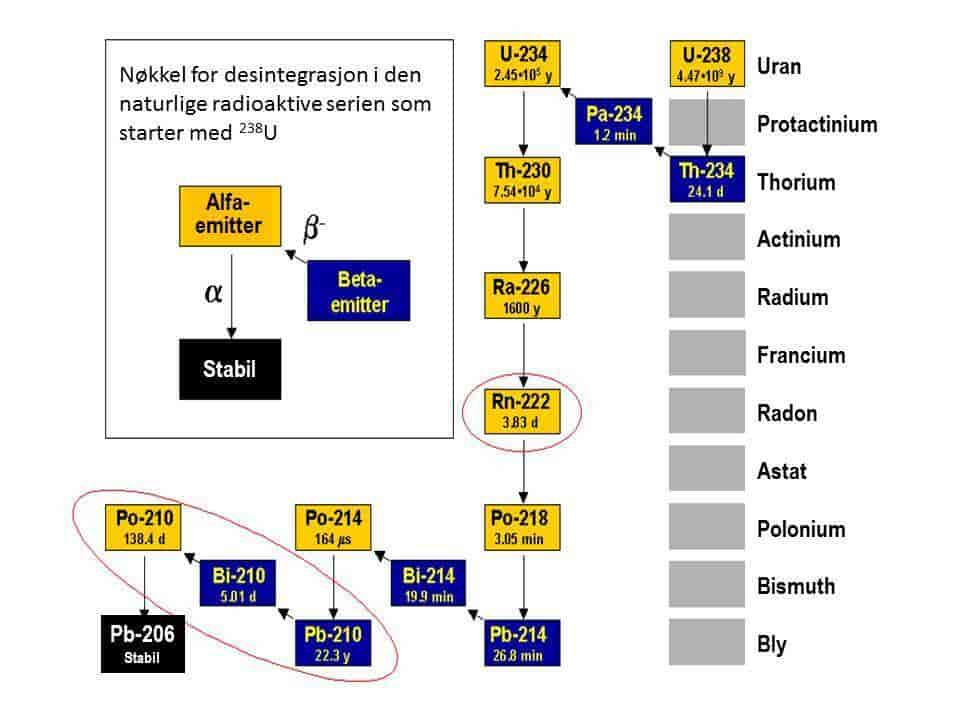
Eksempel: Radionukliden 238U omdannes etter utsendelse av totalt 8 α-partikler og 6 β-partikler til den stabile blyisotopen 206Pb (halveringstid i parentes), se figur 8:
238U (4,5·109 y) → (α) 234Th (24,1 d) → (β-) 234Pa (1,16 m) → (β-) 234U (2,45·105 y)→ (α ) 230Th (7,54·104 y) → (α) 226Ra (1600 y) → (α) 222Rn (3,82 d) → (α) 218Po (3,098 m) → (α) 214Pb (26,8 m) → (β-) 214Bi (19,9 m) → (β-) 214Po (163,6 μs) → (α) 210Pb (22,2 y) → (β-) 210Bi (5,012 d) → (β-) 210Po (138,38 d) → (α) 206Pb (stabil)
På tilsvarende måte vil radionukliden 235U etter 7 α- og 4 β-desintegrasjoner bli omdannet til stabilt bly, 207Pb:
235U → (7α + 4β-) 207Pb (stabil)
og radionukliden 232Th etter 6 α- og 5 β-desintegrasjoner omdannes til stabilt bly, 208Pb:
\[\ce{^210_83Bi ->[\beta] ^210_84Po ->[\alpha] ^208_82Pb} \text{ (stabil)}\]
Det eksisterer også en fjerde serie, som begynner med neptunium 237Np og etter 8 α- og 4 β-desintegrasjoner slutter med stabilt thallium, 205Tl:
237Np → (8α + 4β-) 205Tl (stabil)
238U-serien kalles også uran-radium-serien eller (4n + 2)-serien. Den er karakterisert ved at alle nuklider i serien har nukleontall 4n + 2, der n er et helt tall. På tilsvarende måte kalles 235U-serien for uran-actinium-serien eller (4n + 3)-serien og 232Th-serien for thoriumserien eller 4n-serien. Den fjerde serien, neptuniumserien, med nukleontall 4n + 1 forekommer ikke i naturen fordi ingen nuklider i denne serien har lengre halveringstid enn to millioner år.
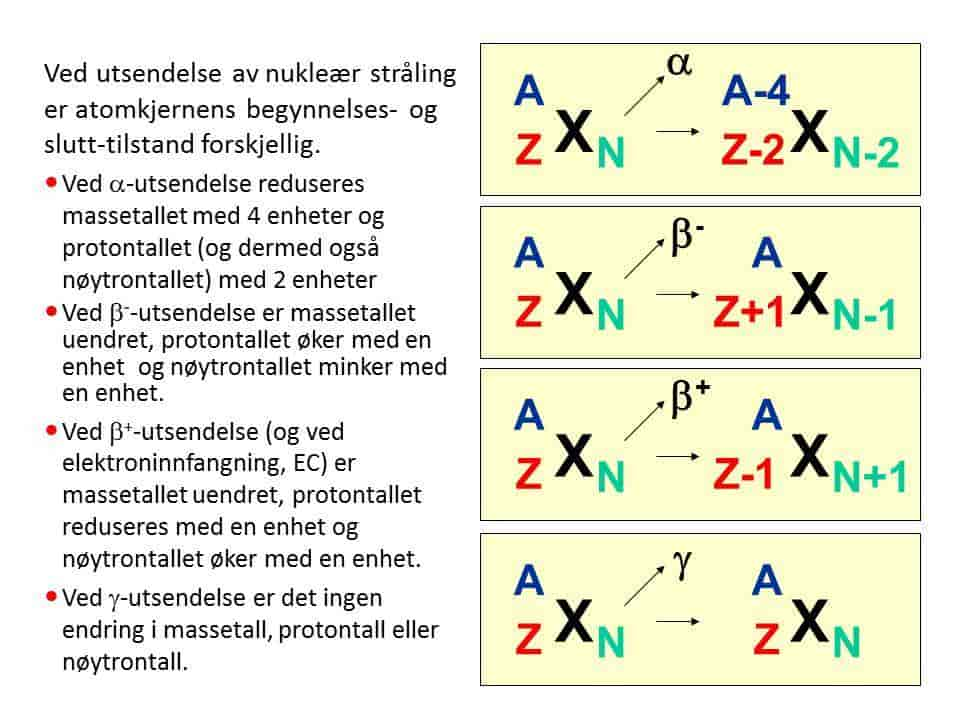
Fordi atomnummeret Z av og til forandres med 1 (ved β-desintegrasjon), av og til med 2 (ved α-desintegrasjon), kan samme verdi av Z, det vil si samme grunnstoff, opptre i alle seriene og også to ganger i samme serie, etter en α- og to følgende β-desintegrasjoner. Se også grunnstoffomdanning.





Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.