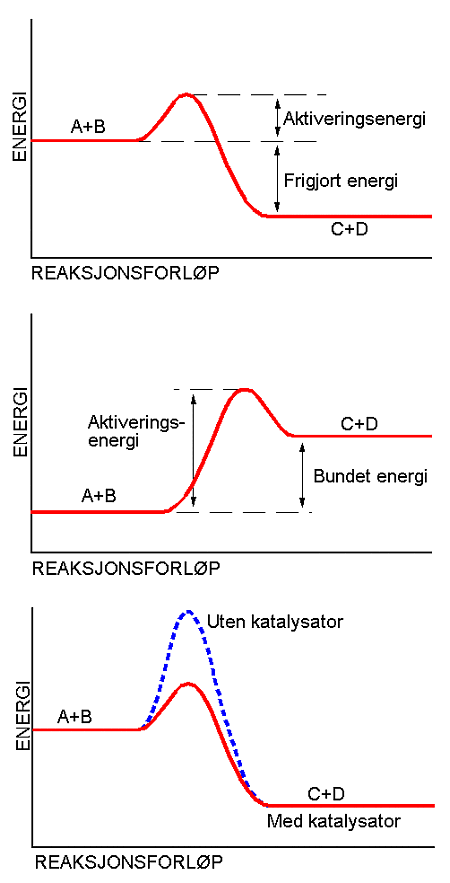
Aktiveringsenergi er den energien som utgangstoffene (reaktantene) må ha for at en kjemisk reaksjon skal kunne skje.
Aktiveringsenergien kan beregnes som forskjellen i energi mellom utgangsenergien og energien til det aktiverte komplekset, altså det mest energirike mellomstadiet under reaksjonen.
Energien hos reaktantene vil normalt være langt lavere enn aktiveringsenergien, men fordi energien er ujevnt fordelt mellom reaktantene (Maxwell-Boltzmanns fordelingslov), og fordi energien hele tiden utveksles dem imellom, så vil etter en viss tid alle reaktantene kunne ha fått høy nok energi, og reaksjonen vil være avsluttet.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.