Fosfor er et grunnstoff som har mange funksjoner i fysiologien. I kroppen foreligger fosfor ofte som fosfat. Omtrent 80 prosent av alt fosfor i kroppen finnes i skjelettet. Det er også en viktig bestanddel i DNA.
- Les mer om fosfor – grunnstoff

Fosfor er et grunnstoff som har mange funksjoner i fysiologien. I kroppen foreligger fosfor ofte som fosfat. Omtrent 80 prosent av alt fosfor i kroppen finnes i skjelettet. Det er også en viktig bestanddel i DNA.
Et voksent menneske inneholder rundt 700 gram fosfor i form av fosfater. Rundt 80 prosent av dette finnes i skjelettet, men det finnes også i nervevev, hår, tenner og i organismen for øvrig. Fosfat finnes også i urin.
Det daglige behovet er omtrent 1,4 gram hos unge i alderen 12–18 år og omtrent 0,8 gram hos voksne, med et tillegg på 0,5 gram for gravide og ammende. Fosfor fås gjennom melk og melkeprodukter (ost), eggeplomme, fisk, lever, kjøtt, nøtter og poteter.
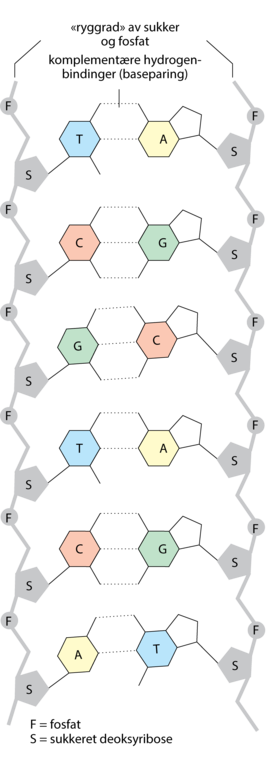
Fosfor er et livsviktig stoff. Salter av fosforsyre kalles fosfater og finnes i organismen dels som uorganiske salter (kalsium- og magnesiumfosfat, særlig i knoklene), dels som bestanddel av tallrike organiske forbindelser, blant annet byggesteinene (nukleotidene) i DNA og RNA. Nukleotider fungerer også som koenzymer. Det viktigste er ATP, som inngår i nesten alle cellens prosesser som leverandør av kjemisk energi.
Gult fosfor er meget giftig. På huden kan det fremkalle svært smertefulle sår som er vanskelige å behandle. Rødt fosfor dannes av gult fosfor ved oppvarming til ca. 250 °C. Det er ikke giftig og antennes først ved cirka 430 °C. Svart fosfor dannes av gult ved oppvarming under høyt trykk. Det er ikke giftig og veldig lite reaksjonsdyktig.
Fosforforgiftning er nå en sjelden forgiftning, men var tidligere vanlig fordi gult fosfor ble brukt til fyrstikker og til rottegift. Brannbomber inneholder også fosfor.
Ved inntak gjennom munnen oppstår det en akutt forgiftning med kvalme, brennende magesmerter og oppkast. I typiske tilfeller følger det noen dager med symptomfrihet, og deretter utvikles symptomer på en alvorlig leverskade.
Ved kronisk forgiftning er hovedsymptomene magesmerter, blødninger og knokkelbetennelse som særlig angriper underkjeven. Kronisk fosforforgiftning forekom i industrien.
Aksjoner på fyrstikkfabrikkene på 1800-tallet bidro til at problemet ble mer kjent, og førte etter hvert til også mer generelle arbeidshygienske tiltak. Fosforforgiftning er i dag svært sjelden.

Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.