Nervecellenes aktivitet er avhengig av at det er forskjell i konsentrasjonen av visse kjemiske stoffer på utsiden og innsiden av cellemembranen. Det dreier seg hovedsakelig om natrium-, kalium- og kloridioner (se aksjonspotensial, nerveimpuls). Spesielle egenskaper hos nervemembranen er også viktige.
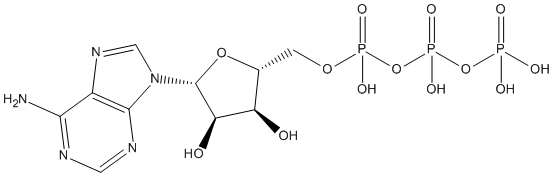
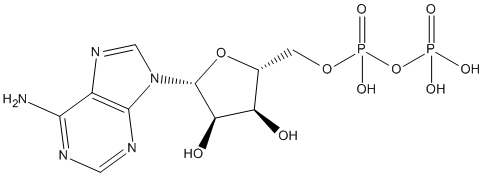
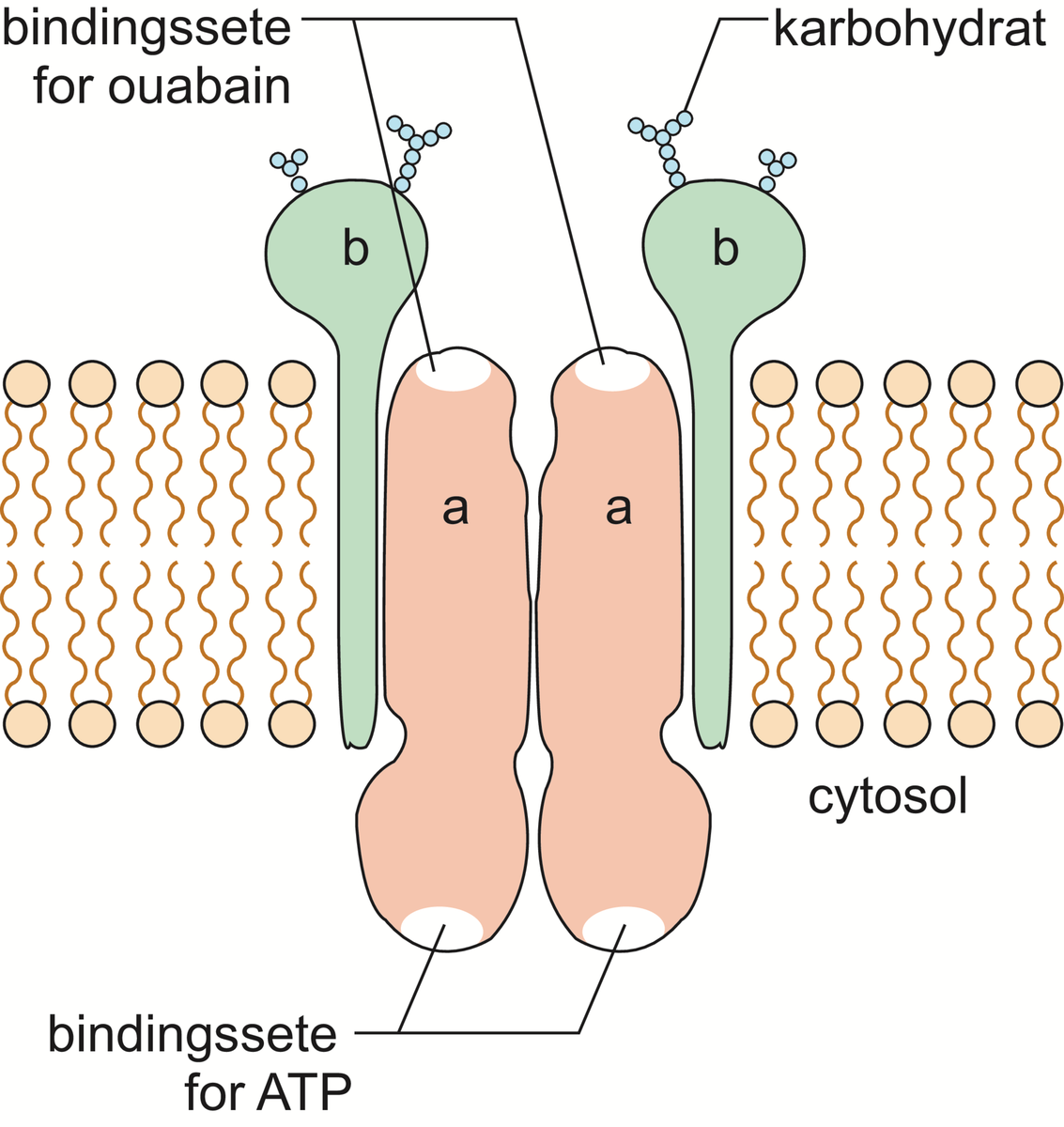
En nervecelle i hvile kan sammenlignes med et ladd batteri, hvor ladningen eller spenningen over membranen opprettholdes av en pumpemekanisme. I denne mekanismen spiller ATP en nøkkelrolle. Pumpemekanismen kalles derfor en enzymatisk ionepumpe. Denne pumpen må være i stand til å transportere kaliumioner inn i cellen og natriumioner ut av cellen. ATP er ansvarlig for denne mekanismen og gjør bruk av et mellomprodukt kalt fosfoprotein.
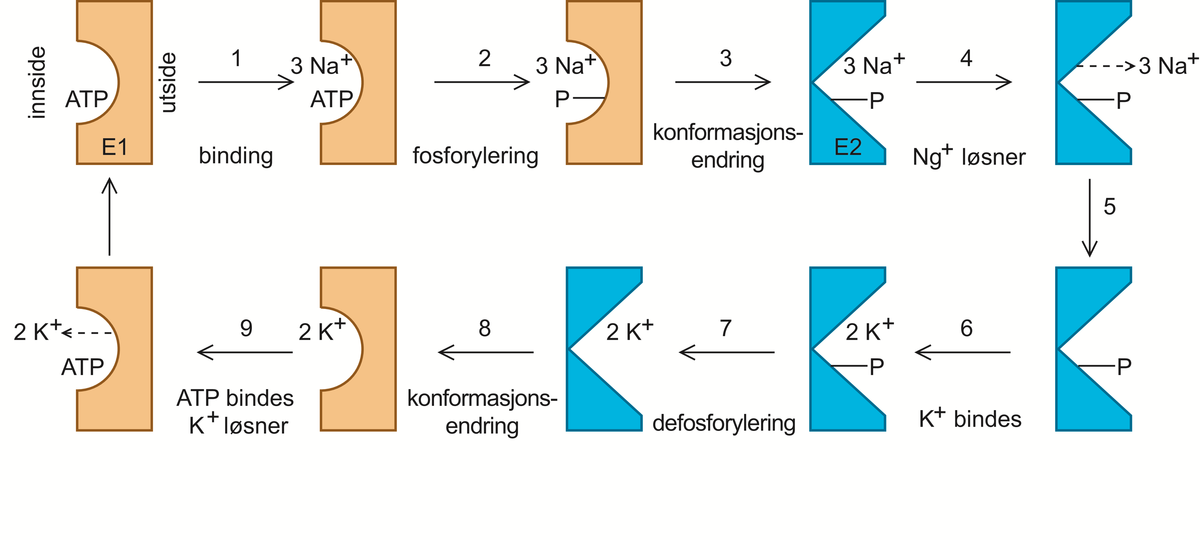
Transporten av ladde partikler foregår i to faser: Den første settes i gang av natriumioner. Fosfoproteinet – et protein med en fosforgruppe – blir tilført en fosfatgruppe fra ATP, det blir fosforylert. Det fører til en binding av natriumioner på innsiden av membranen.
Fosfoproteinkomplekset beveger seg fra innsiden til yttersiden av membranen. I den andre fasen blir fosfoproteinkomplekset defosforylert, og natriumionet spaltes av, samtidig som et kaliumion bindes. Molekylet beveger seg igjen, denne gangen fra yttersiden til innsiden av membranen og blir på ny fosforylert. To andre enzymer deltar i denne prosessen, nemlig kinase på innsiden av membranen og fosfatase på utsiden.
Den enzymatiske ionepumpen er meget følsom for alle slags ytre påvirkninger. Hvis hjernen ikke får tilførsel av oksygen innen tre minutter, hvilket kan skje for eksempel ved et alvorlig hjerteinfarkt, settes den enzymatiske pumpen ut av spillet. Dette fører til nedsatt funksjon og i senere stadier til at deler av hjernen dør.
Pumpen er også meget følsom for karbonmonoksid, og bevisstløsheten som inntrer ved selv lette forgiftninger, kan tilskrives den skadelige effekten av gassen. Giften cyanid har en direkte effekt på dannelsen av ATP. Forskning på disse mekanismene har bidratt til å gi en molekylær forklaring på flere alvorlige sykdommer i sentralnervesystemet.
I tillegg til de meget viktige prosessene som er nevnt ovenfor, er ATP også uunnværlig for sammenkoblingen av aminosyrer til proteiner (proteinsyntese) og for kopiering av arvematerialet (DNA) i celler som skal dele seg.




Kommentarer (2)
skrev Inga Baadshaug Eide
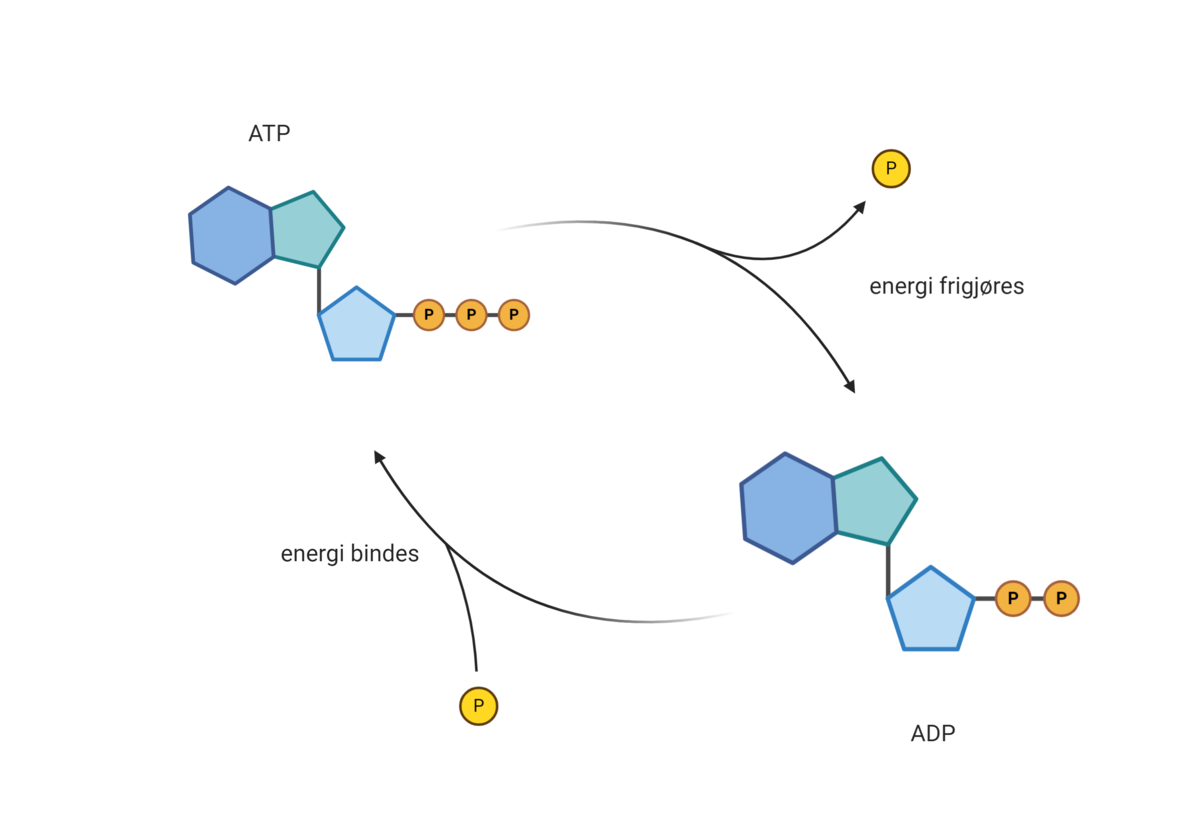
Er det riktig å ha negativt fortegn på energien på høyre side av ATP->ADP-ligningen?
svarte Halvard Hiis
Hei! Ja, det er riktig at det skal være negativt. Jeg har skrevet det om, i håp om at det er lettere forståelig. Fagansvarlig for proteiner, Gustav Vaaje-Kolstad skrev til meg: "Når det gjelder ditt spørsmål om energien som er oppgitt for ATP hydrolyse er det riktig at minustegnet er der da energien som indikeres er endring i Gibbs fri energi (deltaG). En negativ deltaG betyr frigivelse av energi for en reaksjon (altså en eksoterm reaksjon). Kanskje lurt skrive dette i teksten og fjerne energien fra reaksjonslikningen." Hilsen Halvard i redaksjonen
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.