Nerveimpuls er et kortvarig elektrisk signal (aksjonspotensial) som kommer i stand ved strøm av elektrisk ladede ioner over overflatemembranen i nervecellenes aksonutløpere.
nerveimpuls
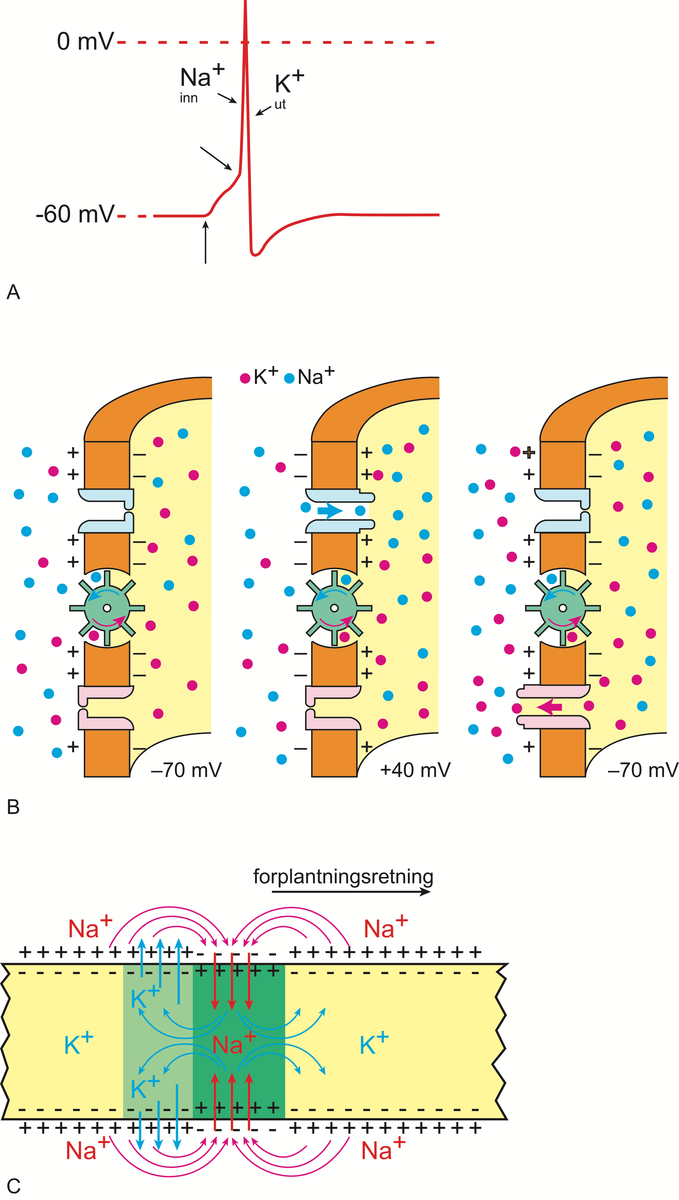
Nerveimpuls.
A) Nerveimpuls, målt som forandring av membranpotensial i en nervecelle, som en funksjon av tiden. Impulsen utløses av en depolarisering fra hvile-membranpotensial (vertikal pil). Denne utløser nerveimpulsen når terskelen for impuls er nådd (første skrå pil). Impulsen består av raske og kortvarige ionestrømmer over cellemembranen (Na+ inn, K+ ut). Aksjonspotensialet, er den kortvarige (noen millisekunder) skarpe forandringen i membranpotensial.
B) Ionestrømmer gjennom cellemembranen går via ionekanaler.
C) Impulsledning. Lengdesnitt av et akson og øyeblikksbildet av en nerveimpuls (grønn sone) under forplantning av impulsen fra venstre til høyre langs aksonet. Samtidig vises fordelingen av elektriske ladninger og de ionene (Na+, K+) som er mest direkte ansvarlige for impulsens ledning. På det aktuelle tidspunkt er nerveimpulsen til stede i det grønnfargede området av aksonet. Her er Na+-ionekanalene åpne, og Na+ strømmer inn i cellen. Derved oppstår elektriske spenningsforskjeller også i væskene på ut- og innsiden av aksonet. Derved får vi ionestrømmer også i aksonets lengderetning. Disse vil føre til en depolarisering av membranen videre i forplantningsretningen. Slik vil impulsen forplante seg kontinuerlig, langs hele aksonet med konstant styrke, og med konstant ledningshastighet så lenge aksonet er jevntykt. Impulsen vil ikke kunne forplante seg i motsatt retning, fordi aksonet her er refraktært (lys grønn sone). Figuren viser impulsledningen i et umyelinisert akson. Impulsledningen i myeliniserte aksoner skjer i prinsippet på samme måte.
Dannelse
Disse membranstrømmene skyldes først og fremst at natrium (Na+)- og kalium (K+)-ioner er ulikt fordelt over cellemembranen. Skjevfordelingen av ionene skyldes en biokjemisk transportmekanisme (Na/K-pumpen). Denne transporterer Na+-ioner fra aksonets innside (aksoplasma) over membranen og ut i den ekstracellulære væsken omkring cellene. Samtidig transporteres K+-ioner fra vevsvæsken og inn i aksoplasma. Derved blir konsentrasjonen av K+-ioner høy intracellulært og konsentrasjonen av Na+-ioner høy i den ekstracellulære væsken. I hvile er membranens gjennomtrengelighet (permeabilitet) langt større for K+- enn for Na+-ioner. Derved oppstår en elektrisk spenningsforskjell over membranen.
Hvilemembranpotensialet
Aksoplasma er elektrisk sett circa 70 millivolt (mV) negativ i forhold til ekstracellulærvæsken. Dette kalle for hvilemembranpotensialet. Disse ionekonsentrasjonsforskjellene og hvilemembranpotensialet representerer drivkreftene for nerveimpulsen. Den oppstår fordi permeabiliteten for ioner blant annet er avhengig av den elektriske spenningsforskjellen over cellemembranen. I hvile er permeabiliteten for Na+-ioner liten og permeabiliteten for K+-ioner mye større.
Overflatemembranen i alle celler består hovedsakelig av fettstoffer (lipider) og er derfor lite permeabel for vann og vannløselige substanser (blant annet ioner). Den aktuelle ionepermeabiliteten kommer i stand ved at spesielle proteiner danner små kanaler gjennom overflatemembranen, såkalte ionekanaler. Proteinenes egenskaper gjør at ulike ionekanaler blir spesielt permeable for bestemte aktuelle ioner (Na+, K+, Ca2+, Cl-), og i tillegg kan rørdimensjonene forandres slik at kanalene kan være åpne eller lukket for passasje for sitt spesielle ion, i mange tilfeller avhengig av det elektriske potensialet over cellemembranen.
Depolarisering
Når membranpotensialet reduseres (depolarisering), det vil si at innsiden av cellen blir mindre negativ, øker gjennomtrengeligheten for Na+-ioner. Disse vil derfor strømme inn i aksonet. Na+-ionene bærer med seg en positiv elektrisk ladning som ytterligere depolariserer membranen, og Na+-permeabiliteten øker videre. Dette blir derved en selvforsterkende prosess, og Na+-ioner fortsetter å strømme inn i aksonet inntil det elektriske potensialet i aksoplasmaet er tilstrekkelig positivt til å forhindre ytterligere Na+-strøm over membranen. Dette hendelsesforløpet er kjernepunktet i dannelsen av nerveimpulsen.
Repolarisering
Den økte permeabiliteten for Na+-ioner varer imidlertid bare ca. 1 millisekund før Na+-kanalene igjen lukker seg. Da har imidlertid andre ionekanaler som er spesielt permeable for K+-ioner, åpnet seg, slik at K+-ioner nå vil strømme ut over membranen og ta med seg positive ladninger slik at hvilemembranpotensialet reetableres, oftest etter 1–2 millisekunder, litt forskjellig i ulike typer av nerveceller. Dette kalles for repolarisering.
Denne sekvensen av kortvarige elektriske ionestrømmer over membranen inngår i dannelsen av nerveimpulsen i de fleste nerveceller.
Overføring
Nerveimpulser dannes normalt like ved aksonets utspring fra nervecellelegemet (aksonutspringskjeglen). Som nevnt fører det til en kortvarig reversjon av membranpotensialet i det aktuelle området. Derved blir det en elektrisk spenningsforskjell på langs i aksoplasma, og denne vil drive langsløpende ionestrømmer i aksonet. Disse strømmene vil depolarisere naboområdet av aksonet og føre til en innadrettet Na+-strøm her. Den lokale Na+-permeabiliteten aktiveres, og alle prosessene i impulssekvensen gjentas i det tilgrensende området, og i neste omgang videre langs aksonet. Signalet forplanter seg videre som en kortvarig reversjon av hvilemembranpotensialet i hele aksonets utstrekning. Energien som trengs til forplantningen, stammer fra den kortvarige utvekslingen av Na+- og K+-ioner sekvensielt i hvert lille segment av aksonet. Styrken på impulsen opprettholdes derfor i hele forløpet.
Hastighet
Forplantningshastigheten av signalet varierer i ulike typer av aksoner. En viktig faktor er aksondiameteren: Tykke aksoner (diameter 15–20 μm) leder impulsene raskere enn tynne aksoner (1–2 μm). Dertil kommer at de tykke aksonene er utstyrt med en ekstra isolasjon (myelin) dannet av gliaceller. Myelinet danner en serie med isolerende skjeder av omtrent 1 mm lengde med bare små åpne gap mellom hvert segment. Resultatet er at impulsene hopper fra ett gap til det neste (sprangvis ledning), og ledningshastigheten øker med omtrent en faktor av 10. De raskest ledende myeliniserte aksoner i nervesystemet har ledningshastigheter på 100–120 m/s, mens de tynneste, umyeliniserte fibrene har ledningshastigheter på 1 m/s eller mindre.
Hemming ved anestesi
Prosessene som driver impulsledningen i nervefibre, kan stoppes ved mange ulike typer kjemiske påvirkninger. Praktisk viktig er injeksjon av lokalbedøvende midler mot smertefulle tilstander eller anestesi i forbindelse med kirurgiske inngrep.


Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.