Immunterapi er kreftbehandling som utnytter kroppens eget immunsystem i bekjempelsen av kreftsykdommen.
Samspillet mellom immunsystemets celler og kreftceller er komplekst. Man vet at immunceller er i stand til å oppdage og ødelegge kreftceller. Imidlertid vet man også at immuncellene i svulstens mikromiljø, altså de tilsynelatende normale immuncellene som omgir svulsten, spiller en viktig rolle i kreftutvikling. Kroppens immunsystem kan altså både bidra til å bremse og stimulere kreftcellenes vekst og deling.
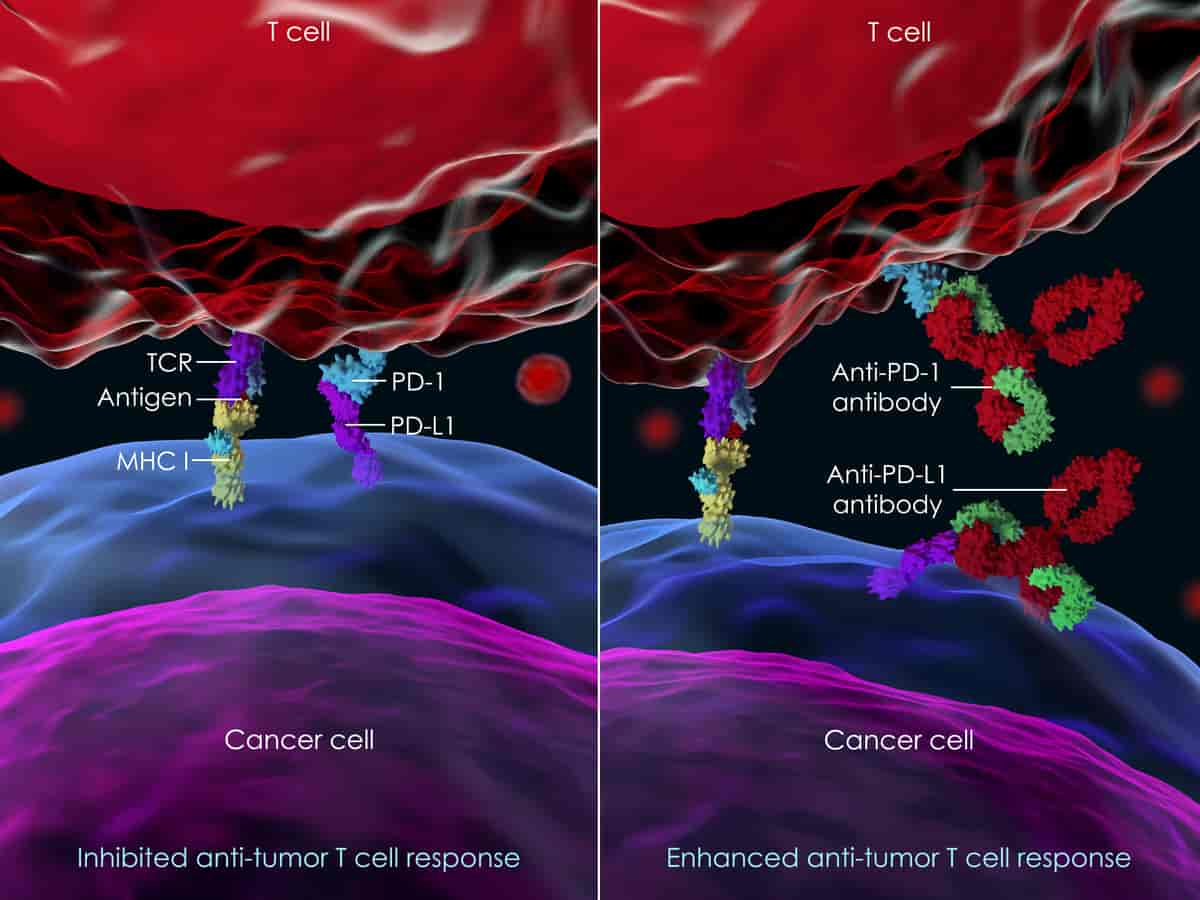
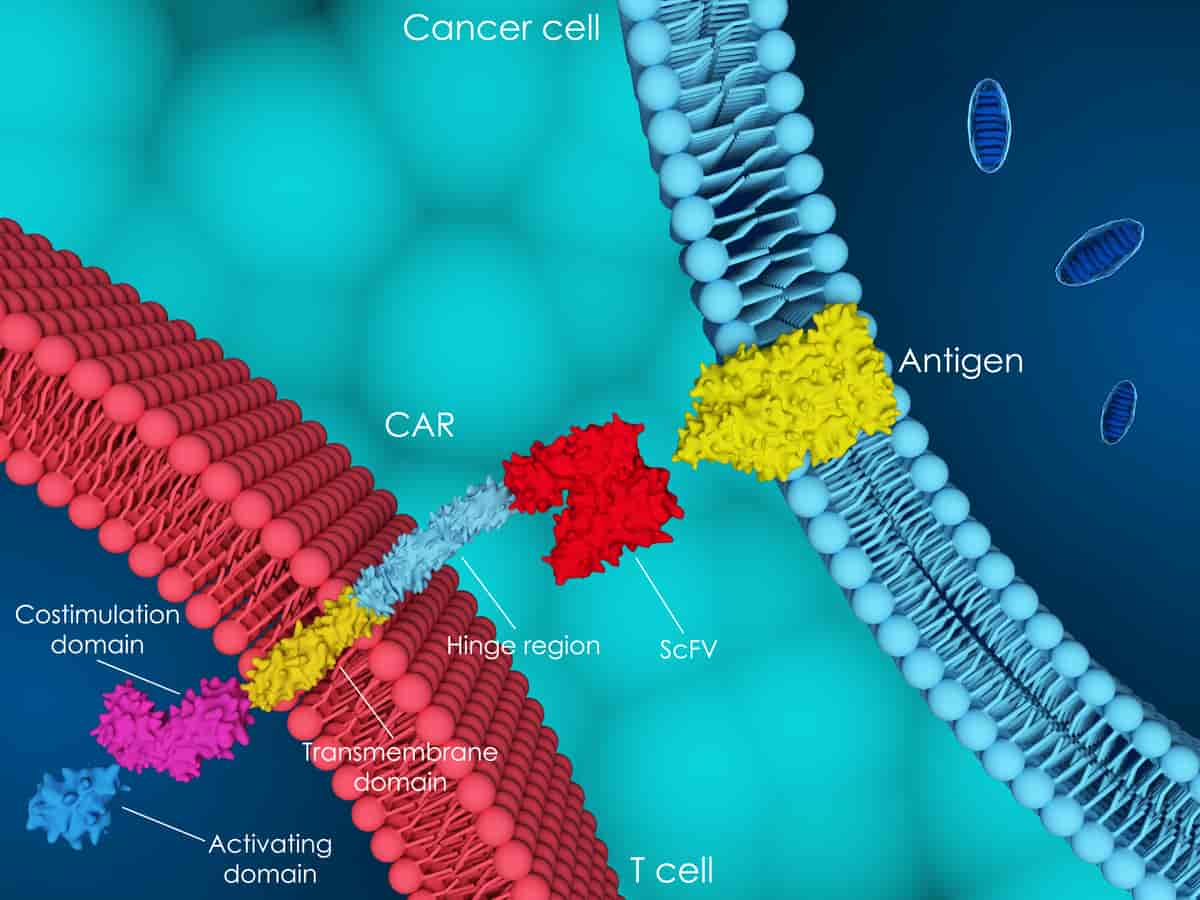
Selv om kreftceller har arvestoff og egenskaper som er svært forskjellig fra normale celler, klarer de likevel å unnslippe «radaren» og unngå at immuncellene oppdager og ødelegger dem. Det har blitt forsket mye på hvordan kreftcellene unngår immunsystemet på denne måten. Etter 2010 har immunterapi fått sitt gjennombrudd i moderne kreftbehandling. De to metodene som har kommet lengst, er såkalte sjekkpunkthemmere («checkpoint inhibitors») og T-celler med kimære antigenreseptorer («CAR-T cells»).



Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.