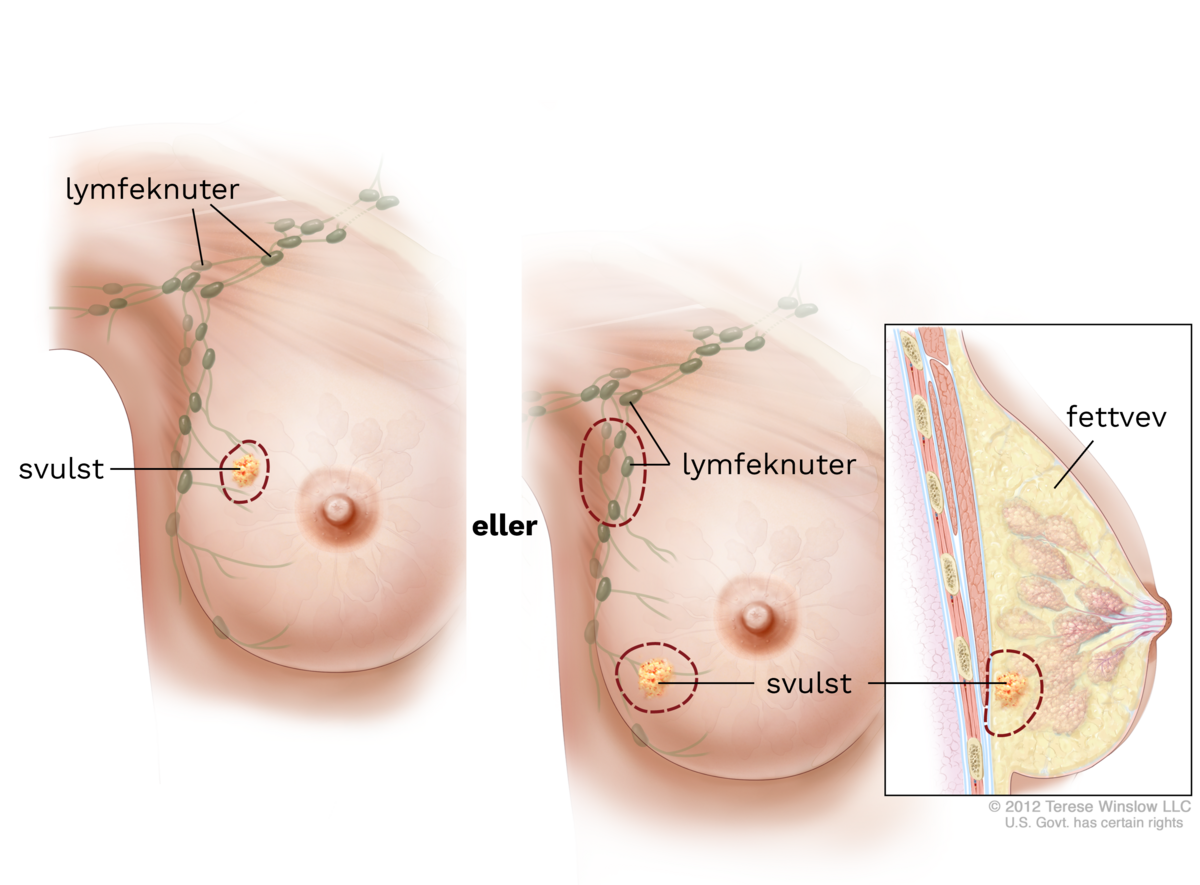
Brystkreft er en ondartet svulst (kreft) i brystkjertelvevet. Det er den vanligste typen kreft blant norske kvinner. Omtrent én av ti kvinner vil utvikle brystkreft en gang i løpet av livet.
Faktaboks
- Også kjent som
-
mammacancer, latin cancer mammae
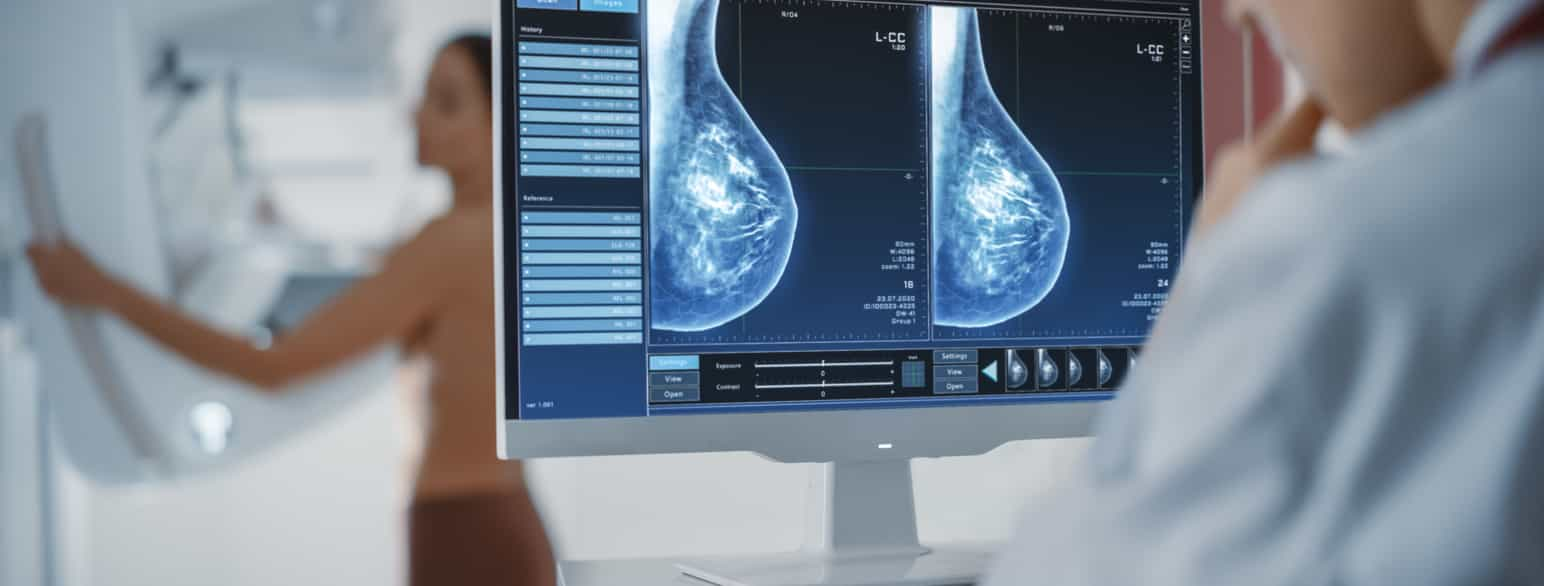
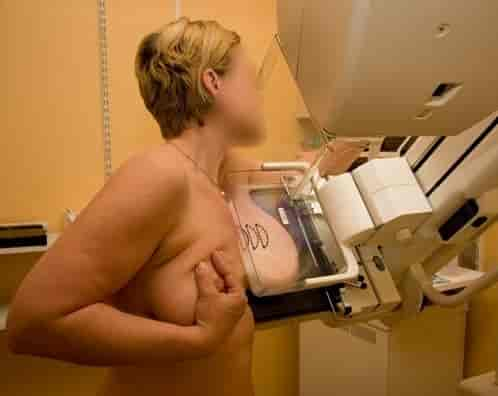
Årsaken til brystkreft er ikke kjent, men det finnes enkelte risikofaktorer og hos noen kan det foreligge en arvelig disposisjon. Første symptom er som regel en kul i brystet, men ofte påvises sykdommen ved rutinemessig mammografi uten symptomer. Alle kvinner i Norge mellom 50 og 69 år får tilbud om mammografiscreening annethvert år.
Behandling er individuelt tilpasset, og kan inkludere operasjon, stråling og cellegift. Brystkreft oppdages ofte på tidlig stadium og da er prognosen god.





Kommentarer (2)
skrev Jørgen Østensjø
svarte Georg Kjøll
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.