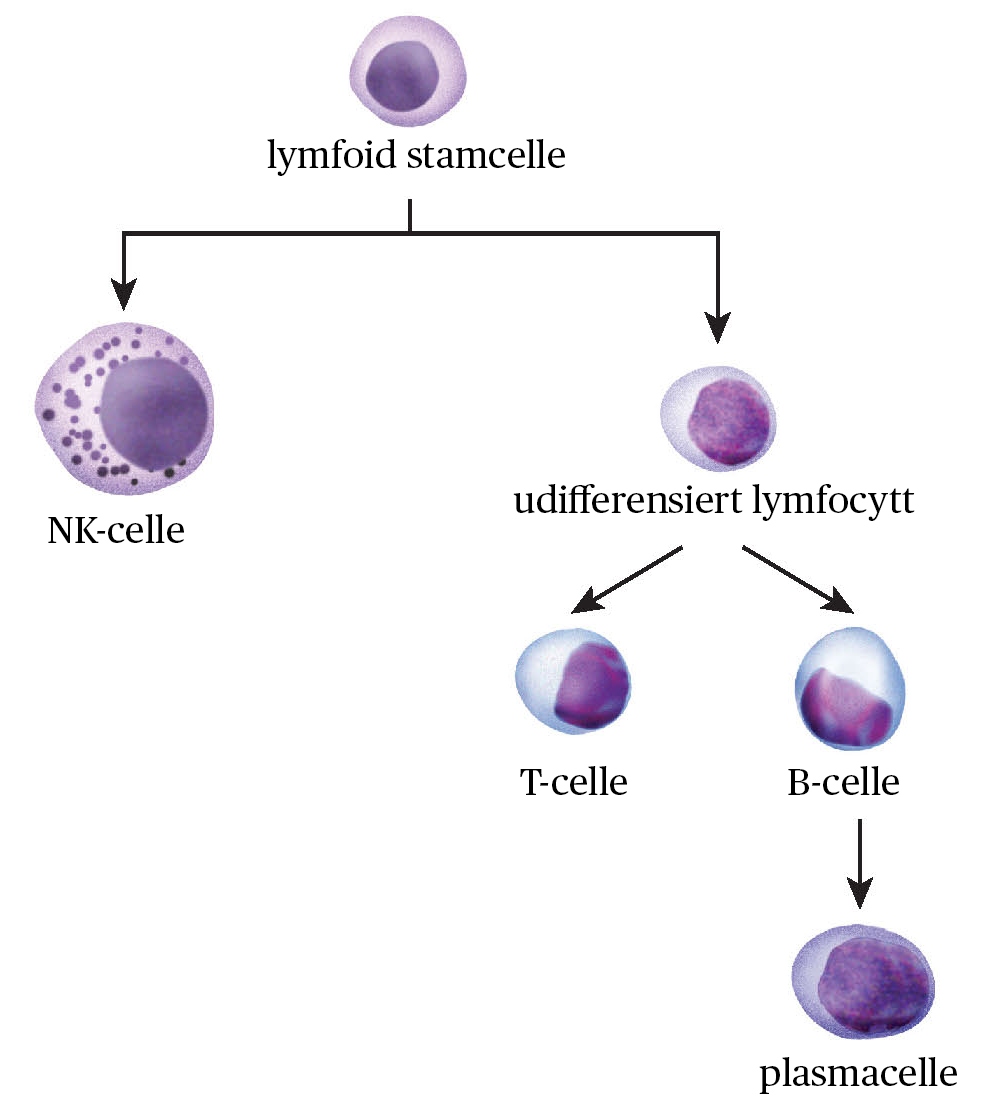
Hvite blodceller, som lymfocytter, utvikles fra stamceller i beinmargen gjennom hele livet. Stamcellene gjennomgår flere modningstrinn før de blir til ferdige celler. Stamcellene vil først utvikles til ett av to forstadier: det lymfoide forstadiet eller det myeloide forstadiet. Det lymfoide forstadiet gir opphav til lymfocytter. Det myeloide forstadiet gir opphav til øvrige typer hvite blodceller, som makrofager og granulocytter.
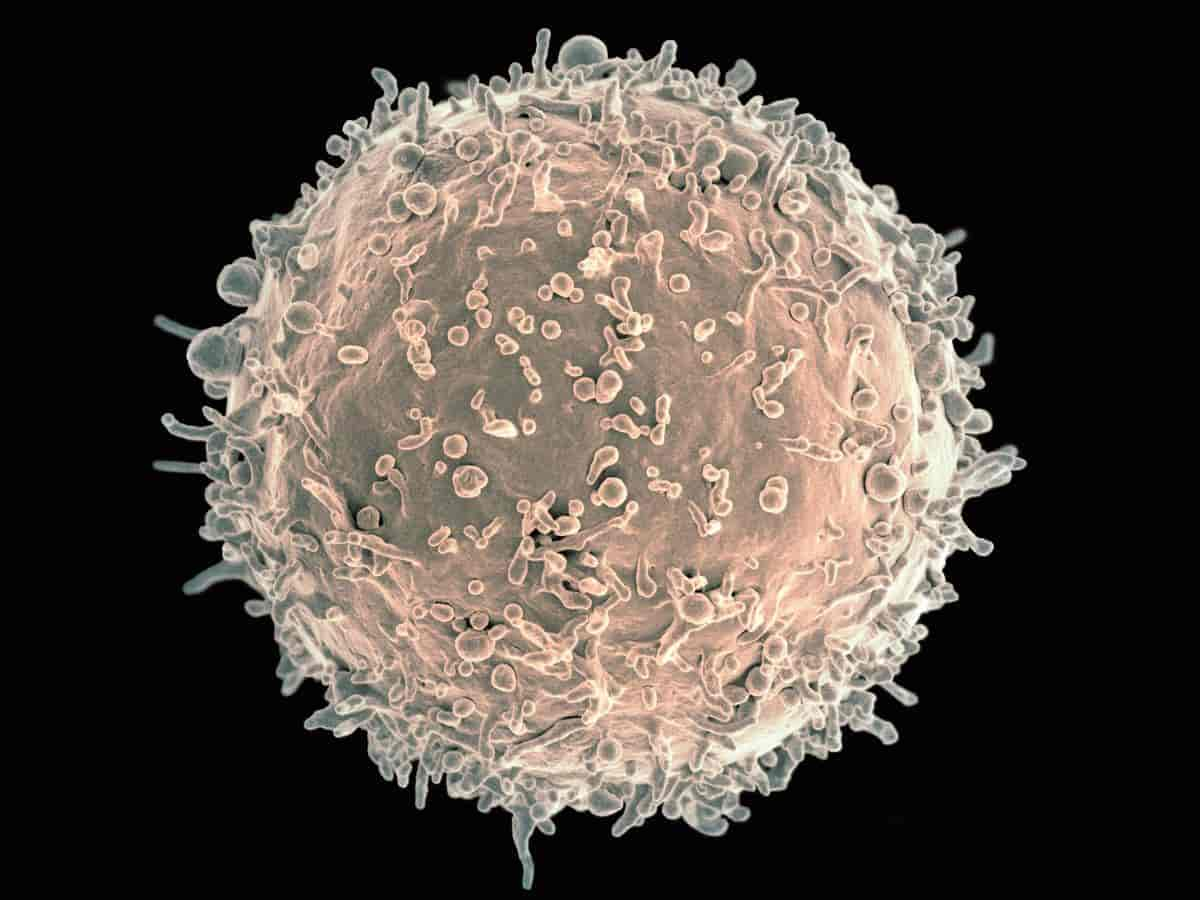
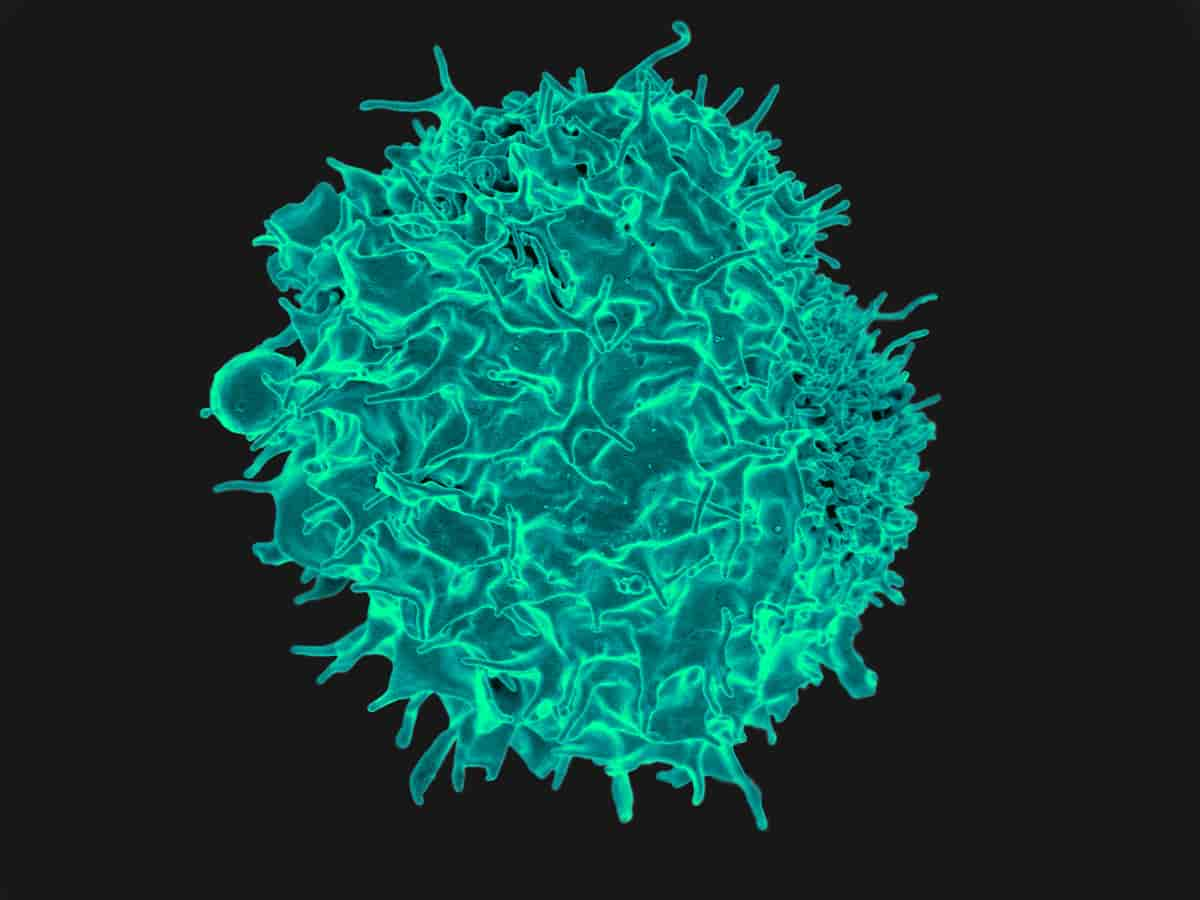
Forstadiene kan modnes videre til bestemte celletyper. Med «modning» menes her at cellen «programmeres» (utvikles) til en konkret celletype, som B-celle eller T-celle, og at den tilegner seg egenskapene den trenger for å utføre denne celletypene funksjoner. Det er hvilke gener som skrus av og på som avgjør hvilken celletype forstadiene modnes til.
Modningen starter i beinmargen, og skjer gjennom flere steg. For B- og T-cellene foregår de siste stegene utenfor beinmargen. T-cellene fullfører sin modning i thymus, derav navnet T-celler. Thymus er et lite organ som ligger mellom hjertet og brystbeinet. Størsteparten av modningen til B-cellene skjer i beinmargen, men enkelte modningstrinn foregår i milten.
Selv om B-cellenes «B» ofte sies å vise til at deres modning i hovedsak skjer i beinmargen, er opphavet til navnet noe annet. B-cellene ble først beskrevet i et spesialisert organ hos fugler, kalt bursa fabricii, og «B» refererer derfor til «bursa». Bursa fabricii finnes ikke hos mennesker.




Kommentarer
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.