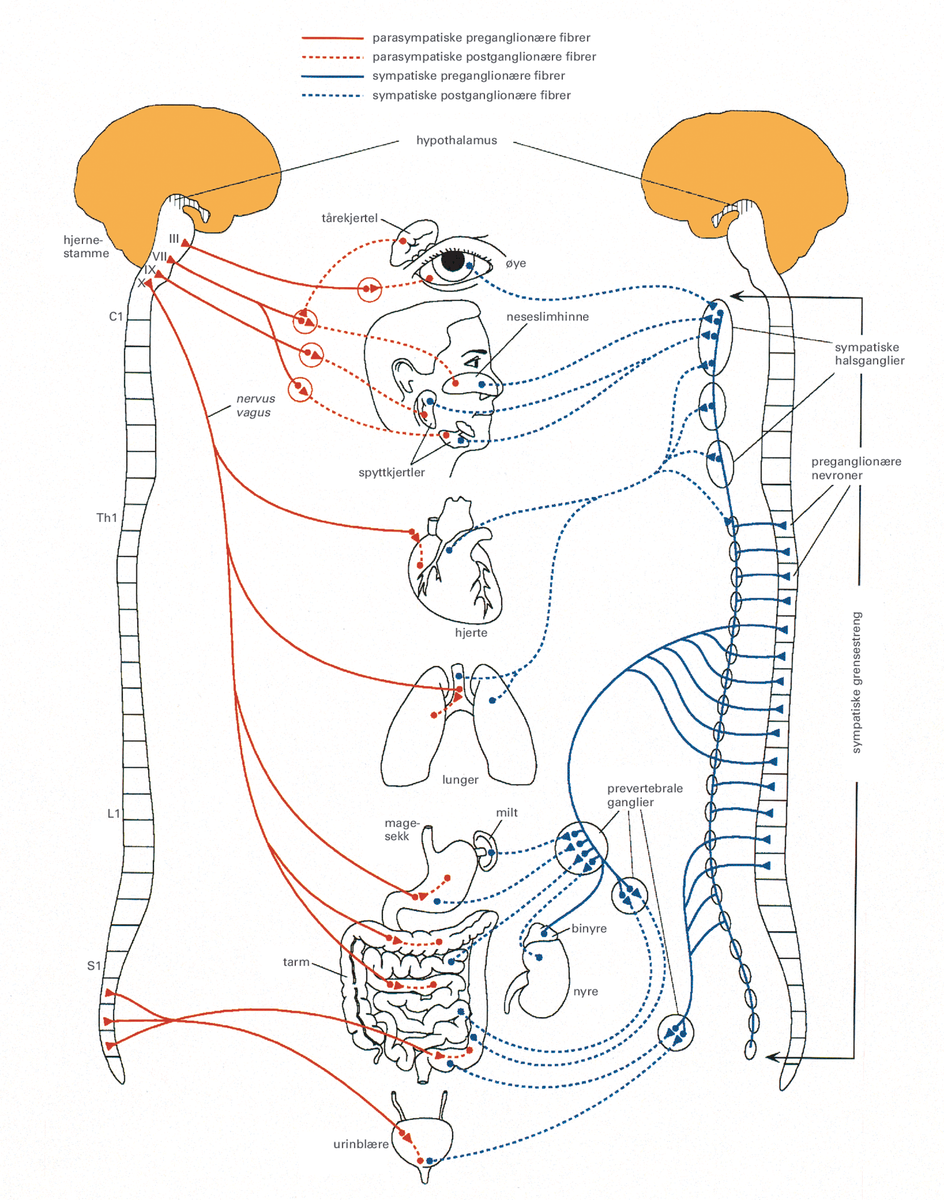
Det autonome nervesystemet er den delen av nervesystemet som styrer aktiviteten i glatt muskulatur, hjertemuskulatur og kjertler, det vil si så godt som alle våre indre organer unntatt de tverrstripete skjelettmusklene.
Autonom betyr selvstyrende. Det betyr i denne sammenhengen at vi ikke har noen direkte, viljemessig kontroll over aktiviteten i denne delen av nervesystemet. Motstykket er det somatiske nervesystemet, altså den delen av nervesystemet som styrer aktiviteten i våre skjelettmuskler, og som gir opphav til våre vanlige bevisste sanseopplevelser. Det er en stor grad av samordning av aktiviteten i disse to delene av nervesystemet. Sammen er de ansvarlige for å tilpasse aktiviteten i de ulike organene til hele kroppens behov.
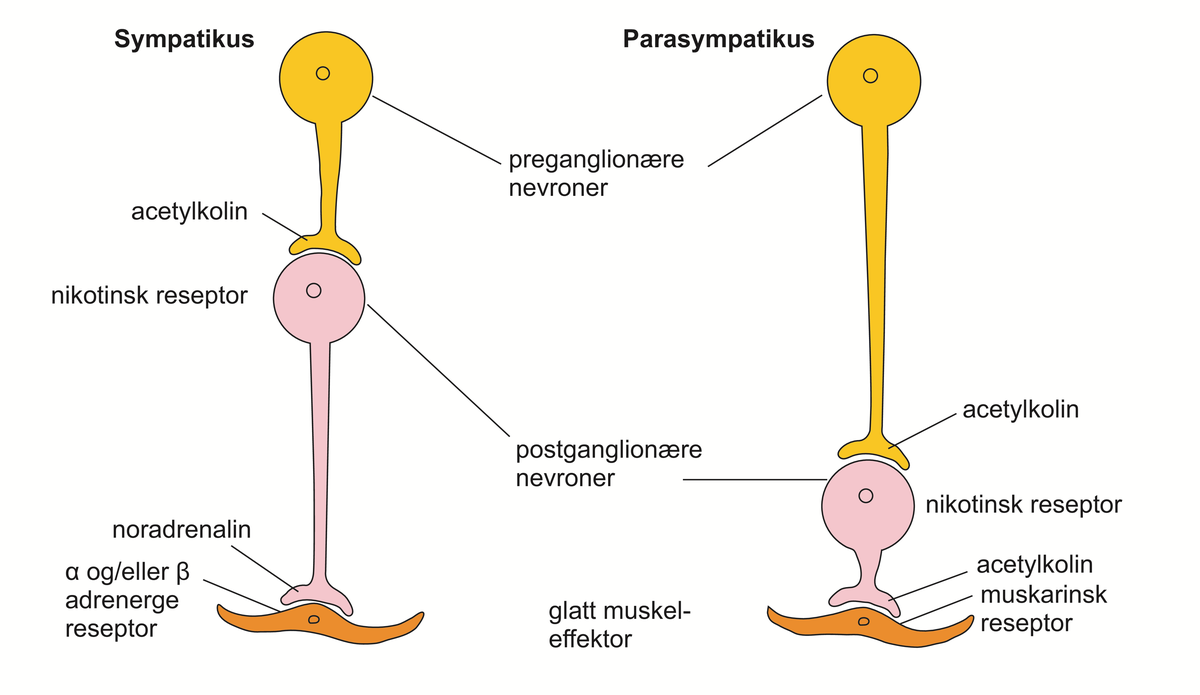
Det autonome nervesystemet består av tre komponenter:
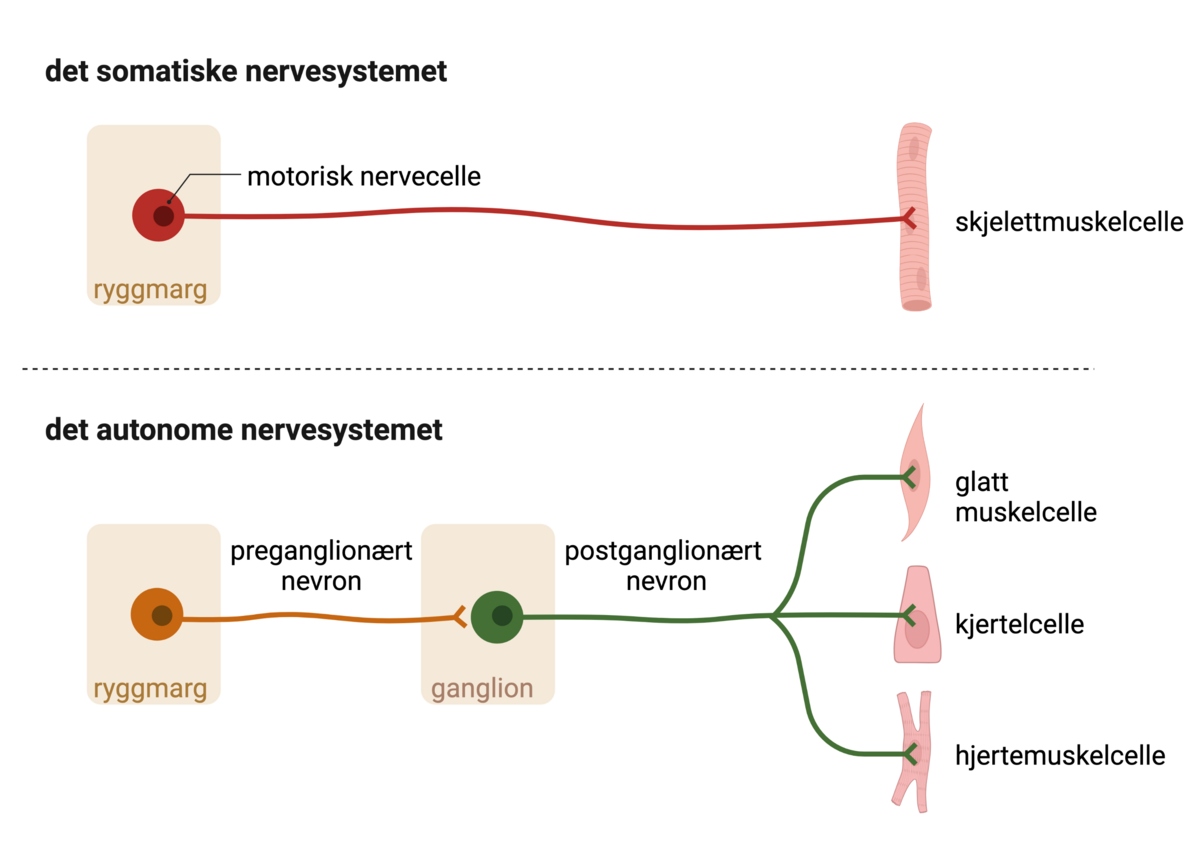
Utenfor hjernen og ryggmargen (sentralnervesystemet) er de tre systemene separate anatomiske enheter, men med koblinger seg imellom. I det autonome nervesystemet er det flere ledd mellom nervecellene fra sentralnervesystemet til målorganene (effektororganene) enn i det somatiske nervesystemet. Effektororgan er det organet som mottar signaler fra en nerve, for eksempel kjertler, glatt muskulatur og hjertemuskulatur. I det somatiske nervesystemet går nervefibrene fra motoriske nerveceller i ryggmargen og hjernestammen direkte til sine tverrstripete skjelettmuskler.




Kommentarer (2)
skrev Kjersti Østlie
svarte Marte Ericsson Ryste
Kommentarer til artikkelen blir synlig for alle. Ikke skriv inn sensitive opplysninger, for eksempel helseopplysninger. Fagansvarlig eller redaktør svarer når de kan. Det kan ta tid før du får svar.
Du må være logget inn for å kommentere.